小核酸药物评价模型—B6-hSMN2(SMA)小鼠
2023.11.09本次和大家见面的是脊髓性肌萎缩症(SMA)模型——B6-hSMN2(SMA)小鼠,先让小赛带大家了解一下SMA。
SMA是由脊髓前角细胞运动神经元变性引起的常染色体隐性遗传病,以严重进行性肌无力和肌萎缩为特征,是婴幼儿期常见的致死性罕见遗传病。SMA全球发病率为1/6,000~1/10,000,在罕见病中属较高水平,也被称为罕见病中的“常见病”[1]。
多数SMA由SMN1突变导致
SMA与生存运动神经元(SMN)蛋白有关,该蛋白缺乏会在脊髓运动神经元中导致广泛的剪接缺陷和功能缺失。人体SMN编码基因分为SMN1和SMN2,SMN1通过转录和翻译生成完整功能性蛋白,是体内SMN蛋白的主要来源。SMN2与SMN1高度保守,但在7号外显子剪接增强子处存在一个核苷酸差异,导致生成的多数SMN2 mRNA缺少第7个外显子,编码功能缺失的SMN截断蛋白,并在细胞内迅速降解[2,3]。仅有部分SMN2 Pre-mRNA(10~15%)能被剪切为全长mRNA,编码具有正常功能的SMN蛋白(图1)。
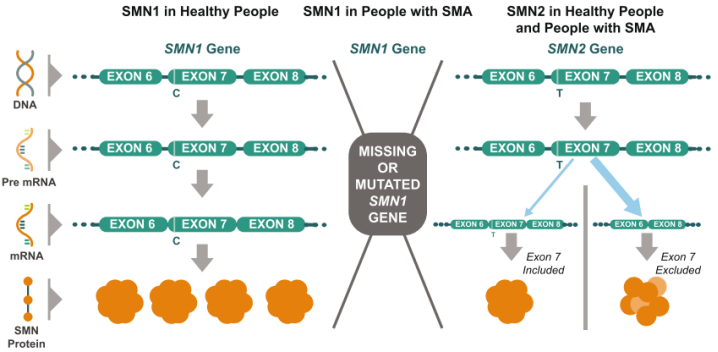 图1 SMN2基因编码的少量功能性SMN蛋白无法完全代偿SMN1基因的缺失[3]
图1 SMN2基因编码的少量功能性SMN蛋白无法完全代偿SMN1基因的缺失[3]
约95%的SMA患者携带SMN1第7号外显子纯合缺失突变或使SMN1转为SMN2的突变,SMN2表达无法代偿体内SMN蛋白的缺失,进而影响运动、呼吸和吞咽并累及脾脏、心脏和胰腺等器官,甚至威胁生命。在SMN1缺失的情况下,根据患者体内SMN2的拷贝数,可将SMA分为0~Ⅳ型。Ⅰ型SMA患者具有2个SMN2拷贝,Ⅱ型SMA患者具有3个SMN2拷贝,Ⅲ型和Ⅳ型SMA患者具有更多SMN2拷贝。一般来讲,患者体内SMN2拷贝数越多,疾病的严重程度越低,Ⅰ型SMA是较为严重的亚型,约占SMA总人群的60%[4-5]。
SMA模型的构建策略
根据小鼠SMN基因特性(仅存在Smn1基因)和多数SMA的遗传特性(SMN2不能代偿SMN1的缺失),赛业生物将小鼠Smn1基因原位替换为人类SMN2基因,构建了SMN1缺失并表达人源SMN2(hSMN2)的Ⅰ型SMA模型(图2)。
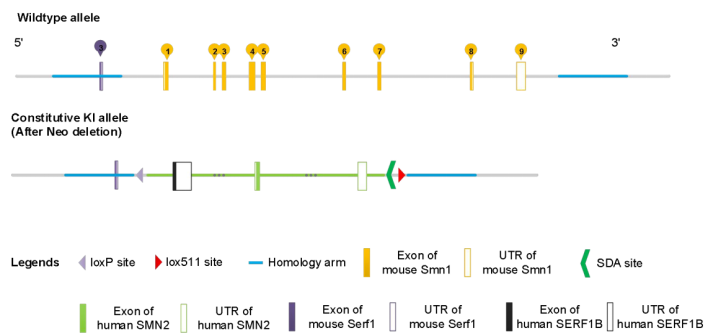
图2 B6-hSMN2(SMA)小鼠基因编辑策略
这种策略模拟大部分SMA的遗传特性,即SMN1纯合缺失和SMN2双拷贝。与敲除小鼠Smn1基因,并通过转基因随机插入若干拷贝SMN2基因的传统策略相比,这种策略不存在SMN2基因随机插入,小鼠拥有清晰的SMN2基因拷贝数并能稳定遗传,符合大多数SMA的情况。此外,本模型可以与在6号染色体插入SMN2基因的Rosa26-hSMN2小鼠交配,增加小鼠体内SMN2拷贝以模拟不同SMA亚型。
B6-hSMN2(SMA)小鼠表达人源SMN2基因,不表达小鼠Smn1基因
与野生型对照组(B6N)相比,纯合B6-hSMN2(SMA)小鼠不表达小鼠Smn1 mRNA(图3 d),其体内同时存在缺少7号外显子(E7-)及包含7号外显子(E7+)的人类SMN2转录本(图3 a-b),SMN2 E7+转录本仅占总SMN2转录本(E7+&E7-)的极少部分(图3 c)。

图3 3周龄B6-hSMN2(SMA)小鼠和野生型小鼠(B6N)基因表达检测
B6-hSMN2(SMA)小鼠缺乏SMN蛋白
基因的改变影响了SMN蛋白水平,与野生型相比,纯合B6-hSMN2(SMA)小鼠脊髓、心脏、骨骼肌、脑部、肝脏和肾脏中仅存在少量由SMN2基因编码的SMN蛋白(图4),这与人类SMA患者体内的蛋白表达模式相似。
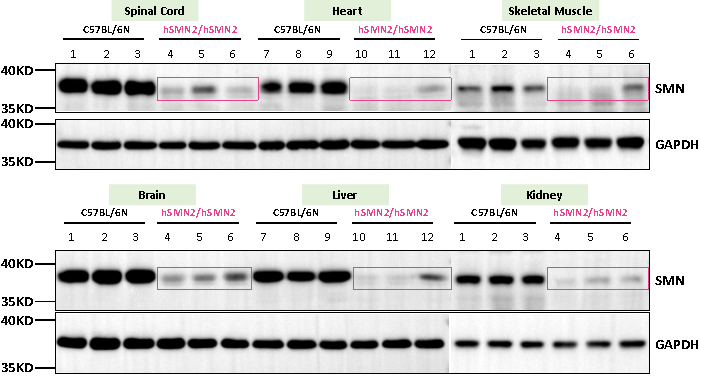
图4 3周龄野生型小鼠(C57BL/6N)和 B6-hSMN2(SMA)小鼠体内SMN蛋白检测
B6-hSMN2(SMA)小鼠呈现多组织病理
组织学检测结果表明,纯合B6-hSMN2(SMA)小鼠显示出肌细胞坏死和萎缩、胞质崩解、淋巴细胞浸润和肌细胞间隔增宽/排列疏松等肌肉组织病理,局部肌纤维坏死溶解/结构消失、结缔组织增生、粒细胞浸润、掌骨断裂和皮下水肿等脚掌和脚趾病理,以及局部皮下水肿、结缔组织排列疏松、血管扩张、肌细胞萎缩并伴有少量淋巴细胞浸润等尾部病理(图5)。
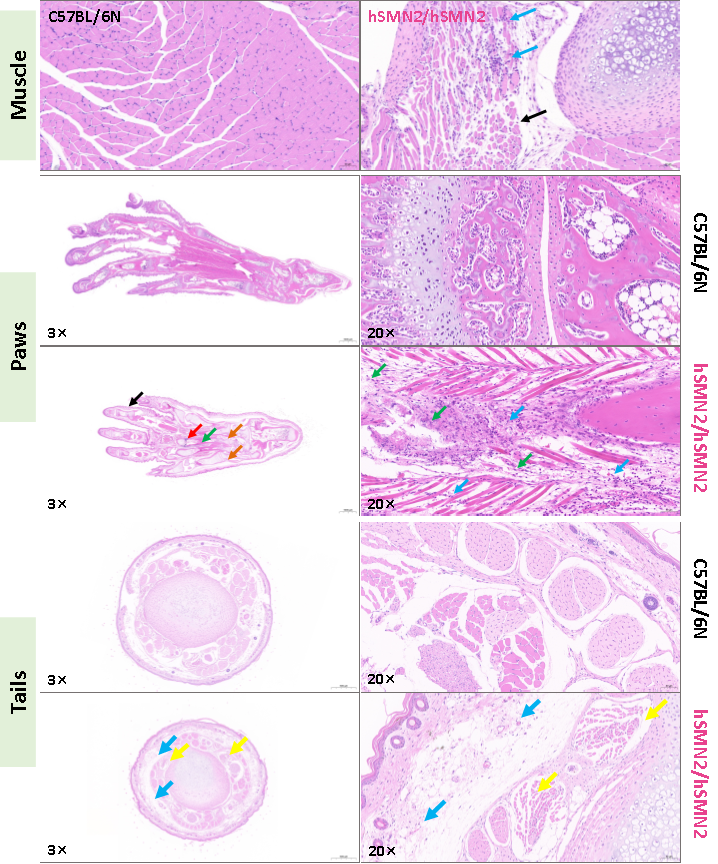
图5 3周龄纯合B6-hSMN2(SMA)小鼠肌肉、脚掌和尾部可见明显病理表型
B6-hSMN2(SMA)小鼠存在严重发育缺陷和渐进性疾病进程
SMN蛋白的缺失导致B6-hSMN2(SMA)小鼠发育出现缺陷,表现为肌肉萎缩、站立不稳、体型较小、身长较短、断尾和四肢浮肿等严重表型(图6)。
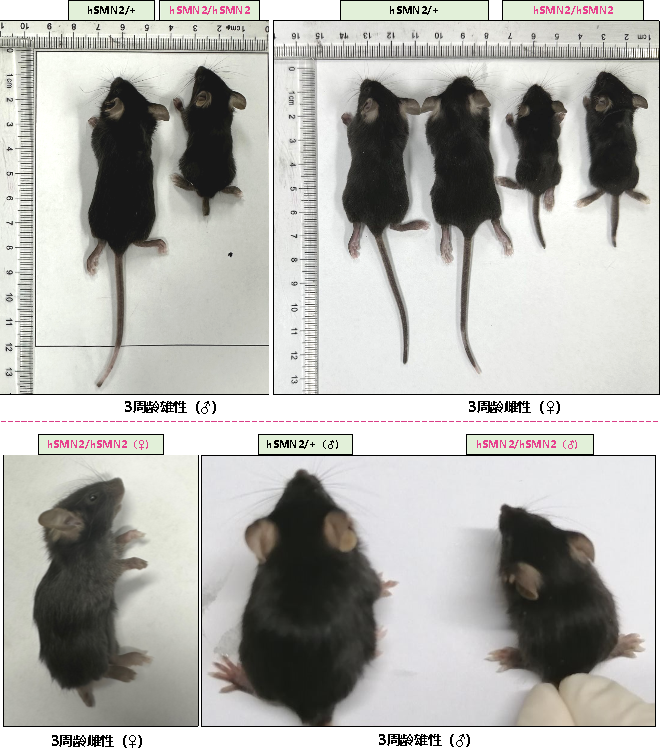
图6 3周龄杂合B6-hSMN2(SMA)小鼠(hSMN2/+)和纯合B6-hSMN2(SMA)小鼠(hSMN2/hSMN2)外观
此外,纯合B6-hSMN2(SMA)小鼠在第20天左右开始死亡,30天左右达到半数致死率。存活的纯合B6-hSMN2(SMA)小鼠在30日龄左右出现脚趾坏死和完全断尾的现象,50日龄左右出现耳朵坏死,66日龄耳朵周围毛发变白(图7)。杂合B6-hSMN2(SMA)小鼠与野生型相似,无异常情况,符合SMA患者的常染色体隐性遗传模式。
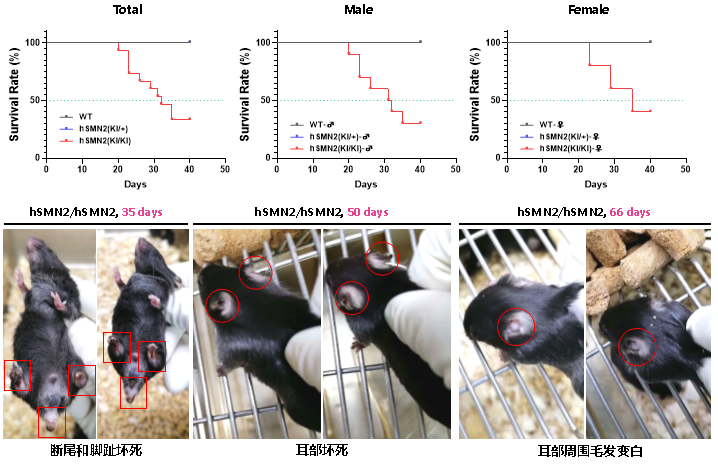
图7 B6-hSMN2(SMA)小鼠生存曲线和疾病进程
小核酸药物减轻B6-hSMN2(SMA)小鼠疾病表型并提高生存率
目前有Zolgensma、Spinraza和Evrysdi三款SMA药物获批上市。Spinraza为首款获批药物,通过反义寡核苷酸(ASO)修饰SMN2 mRNA的剪切模式,使其生成大量包含7号外显子的正常SMN2 mRNA以编码功能性SMN蛋白,这也是SMA治疗的主要方向之一[3]。以Spinraza公开信息为基础合成与其结构和功能类似的反义寡核苷酸(ASO10-27,由GenScript合成),并以脑室内注射(icv)和皮下注射(s.c.)的方式分别给予B6-hSMN2(SMA)小鼠不同剂量的ASO10-27。数据显示,脑室内注射(icv)的ASO可以增加B6-hSMN2(SMA)小鼠脑部SMN蛋白表达量(图8 a)和脊髓前角运动神经元个数(图8 b)。
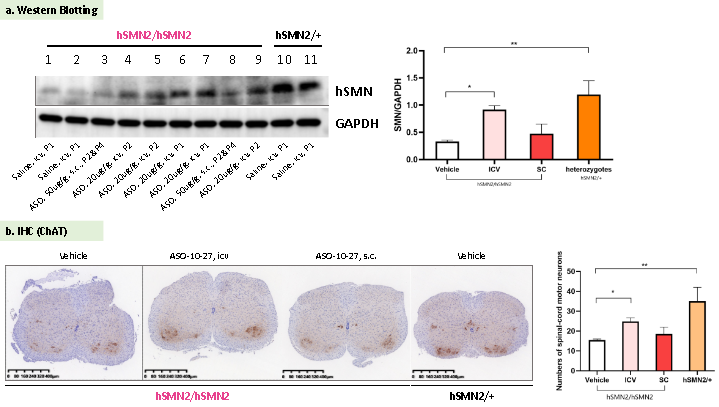
图8 靶向SMN2的ASO对B6-hSMN2(SMA)小鼠SMN蛋白和运动神经元的影响
通过脑室内注射(icv)方式给药的B6-hSMN2(SMA)小鼠生存率明显提升,小鼠在78日龄仍保持存活。未经ASO治疗的B6-hSMN2(SMA)小鼠在35日龄出现脚趾坏死和断尾,ASO治疗组小鼠仅在43日龄出现脚趾轻微肿胀,未见脚趾坏死且尾巴尚存。在78日龄,部分ASO处理组小鼠才出现断尾现象,但仍未见脚趾坏死(图9)。
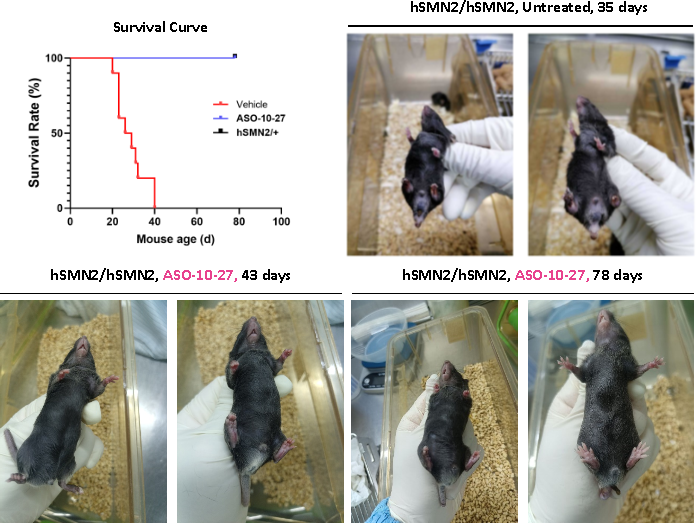
图9 ASO处理提升B6-hSMN2(SMA)小鼠存活率并延缓组织病变
总 结
综上所述,B6-hSMN2(SMA)小鼠表达人类SMN2基因,并存在SMN2 mRNA的选择性剪切,这导致小鼠体内SMN蛋白的缺失,引起与经典SMA模型相似的表型。ASO、siRNA和miRNA等小核酸作为最近几年快速发展新兴药物,因其通过靶向mRNA而非基因来治疗疾病,不存在遗传风险,因此受到众多关注,尤其是遗传性罕见病领域。B6-hSMN2(SMA)小鼠模拟人类SMA的遗传机制和疾病进程,对靶向SMN2的ASO药物具有良好响应,表明本模型可用于靶向SMN2的小核酸及其它类型药物的开发、筛选和评价等研究。


